Ein Stereodeskriptor ist ein als Präfix verwendeter Ausdruck zur Spezifizierung der absoluten oder relativen Konfiguration bzw. der Konformation einer chemischen Verbindung.
Liste der Stereodeskriptoren
| Deskriptor | Schreibweise | Bedeutung | Anwendung | Details |
| +, - | Drehrichtung des polarisierten Lichts; Keine Aussage über die absolute Konfiguration! | |||
| (+)- | rechtsdrehend | |||
| (-)- | linksdrehend | |||
| α, β | Konfiguration am anomeren Zentrum | Anomere | ||
| α- | S-Konfiguration am anomeren C-Atom | |||
| β- | R-Konfiguration am anomeren C-Atom | |||
| ap, sp | Diederwinkel, Torsionswinkel | |||
| sp- | synperiplanar | 0° bis +/-30° | ||
| sc- | synclinal | +/-(30° bis 90°) | ||
| ac- | anticlinal | +/-(90° bis 150°) | ||
| ap- | antiperiplanar | +/- 150° bis 180° | ||
| cis, trans | Relative Stellung von zwei Substituenten bezüglich einer Referenzebene. Siehe auch: E, Z - insbesondere bei mehreren Substituenten | |||
| trans- | Beide Substituenten auf entgegengesetzten Seiten der Referenzebene | |||
| cis- | Beide Substituenten auf der gleichen Seite der Referenzebene | |||
| D, L, DL | Konfiguration eines chiralen Zentrums | Fischer-Nomenklatur | ||
| D- | rechts | |||
| L- | links | |||
| DL- | Racemat | |||
| Delta, Lambda | Δ, Λ | Bezeichnung von stereoisomeren Metallkomplexen und anderen oktaedrischen Komplexen mit drei identischen zweizähnigen Liganden | ||
| E, Z | Relative Stellung von zwei oder mehreren Substituenten bezüglich einer Referenzebene. Siehe auch: cis, trans. Bei mehr als zwei Substituenten werden gemäß CIP-Konvention diejenigen mit der höchsten Priorität ermittelt und betrachtet | |||
| (E)- | Beide Substituenten auf entgegengesetzten Seiten der Referenzebene | |||
| (Z)- | Beide Substituenten auf der gleichen Seite der Referenzebene | |||
| Ent | ent- | Eine Vorsilbe zur Bezeichnung des Enantiomers eines Naturstoffs bzw. verwandten Substanz, bei dem sich der Trivialname nur auf ein bestimmtes Enantiomer bezieht | ||
| erythro, threo | Deskriptor der relativen Konfiguration von Diastereomeren mit zwei asymmetrischen Chiralitätszentren. Eindeutig nur bei Anwendung von Fischer-Projektionen. In unklaren Fällen sollte das l,u oder das R*,S* angewandt werden. | |||
| erythro- | Gleiche Substituenten bzw. Substituenten höchster CIP-Priorität befinden sich auf derselben Seite der Hauptkette | |||
| threo- | Gleiche Substituenten bzw. Substituenten höchster CIP-Priorität befinden sich auf verschiedenen Seiten der Hauptkette | |||
| l, u | Deskriptor der relativen Konfiguration von Diastereomeren mit genau zwei Chiralitätszentren | |||
| l- | Die beiden Chiralitätszentren des Moleküls sind gemäß CIP-Konvention beide R bzw. beide S - also gleich [l für like] | |||
| u- | Die beiden Chiralitätszentren des Moleküls sind gemäß CIP-Konvention unterschiedlich je R und S [u für unlike] | |||
| meso | meso- | Optisch inaktives Mitglied einer Reihe von Stereoisomeren, von denen mindest zwei optisch aktiv sind. Die meso-Verbindung ist trotz des Vorhandenseins von zwei oder mehreren Stereozentren achiral | ||
| P, M | P/M-Nomenklatur zur Benennung der absoluten Konfiguration von Helices, propellerartigen und schraubenförmigen molekularen Einheiten [P von Plus, M von Minus]. | |||
| P- | Rechtsdrehend bei Betrachtung des Moleküls entlang der Drehachse | |||
| M- | Linksdrehend bei Betrachtung des Moleküls entlang der Drehachse | |||
| pro-E, pro-Z | Einer von zwei an einer Doppelbindung gebundenen identischen Gruppen R2 in einer prochiralen Verbindung RR1C=C(R2)2 wird willkürlich eine CIP-Priorität zugewiesen. | |||
| pro-E | Die willkürlich zugewiesene CIP-Priorität von R2 ist höher, als die der anderen identischen Gruppe R2. | |||
| pro-Z | Die willkürlich zugewiesene CIP-Priorität von R2 ist niedriger, als die der anderen identischen Gruppe R2. | |||
| pro-R, pro-S | [[Stereoheterotop]]e Substitutenten werden gemäß CIP-Nomenklatur benannt, indem den beiden identischen Gruppen R2 in der tetraedrischen Gruppe XRR1(R2)2 willkürlich eine CIP-Priorität zugewiesen wird. Diese Methode für die Unterscheidung zwischen stereoheterotopen Gruppen kann auch auf andere Arten von prochiralen molekularen Einheiten oder auf prochirale Teile eines Moleküle angewandt werden. | |||
| pro-R | Die willkürlich zugewiesene CIP-Priorität von R2 ist höher, als die der anderen identischen Gruppe R2. | |||
| pro-S | Die willkürlich zugewiesene CIP-Priorität von R2 ist niedriger, als die der anderen identischen Gruppe R2. | |||
| r, s | Bezeichnung von Substituenten an pseudo-asymmetrischen Zentren, die entsprechend der R/S-Nomenklatur, jedoch mit den kleinen Buchstaben r und s sowie ohne Bindestrich gekennzeichnet werden. | |||
| R, S | Absolute Konfiguration an den Stereozentren von chiralen und insbesondere stereoisomeren Molekülen. Die Prioritäten der Substituenten am Stereozentrum werden gemäß den Prioritätsregeln bestimmt. | CIP-Nomenklatur | ||
| (R)- | Nach Anwendung der Prioritätsregeln sind die Substituenten rechtsläufig (im Uhrzeigersinn) angeordnet. | |||
| (S)- | Nach Anwendung der Prioritätsregeln sind die Substituenten linksläufig (gegen den Uhrzeigersinn) angeordnet. | |||
| rac, racem, (+/-) | rac- | Racemat, Abkürzung für racemo-. | ||
| rel | rel- | Es kann nur die relative, nicht aber die absolute Konfiguration zweier Substitutenten zueinander festgelegt werden. | ||
| s-cis, s-trans | Beschreibung der räumlichen Anordnung zweier konjugierter Doppelbindungen in Bezug auf die dazwischenliegende Einfachbindung. Sollte laut IUPAC nur auf N-Alkylamide angewandt werden. [Anwendung: siehe E/Z] | |||
| sn | sn- | Stereospezifische Nummerierung | Beschreibung der Konfiguration von chiralen Derivaten des Glycerins (Lipid-Nomenklatur, Fette) |
Weitere Deskriptoren für Kohlenhydrate
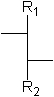
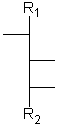
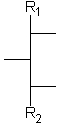
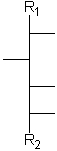
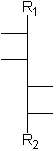
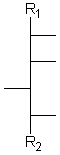
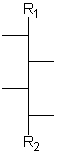
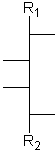
Aldosen mit 3 bis 6 Kohlenstoffatomen und 1 bis 4 aufeinanderfolgenden Chiralitätszentren in Fischer-Projektion.
[Für die Beispiele gilt: R1 = CHO; R2 = CH2-OH; Substituenten = OH]
|
|
|
 |
|
 |
 |
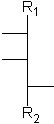 | |
| glycero- | erythro- | threo- | ribo- | arabino- | xylo- | lyxo- | |
| D-Glyceraldehyd | D-Erythrose | D-Threose | D-Ribose | D-Arabinose | D-Xylose | D-Lyxose | |
|
|
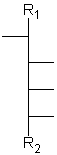 |
 |
 |
 |
 |
 |
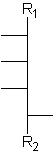 |
| allo- | altro- | gluco- | manno- | gulo- | ido- | galacto- | talo- |
| D-Allose | D-Altrose | D-Glucose | D-Mannose | D-Gulose | D-Idose | D-Galactose | D-Talose |
Quellen
[1] IUPAC Compendium of Chemical Terminology - The Gold Book.
[2] G. P. Moss: Nomenclature of Carbohydrates, Recommendations 1996.
Kategorie: Terminologie
Aktualisiert am 05. Dezember 2017.
Permalink: https://www.internetchemie.info/chemie-lexikon/s/stereodeskriptoren.php
© 1996 - 2024 Internetchemie ChemLin