Magnesiumstearat ist eine chemische Verbindung aus der Gruppe der Salze - im Detail das Magnesium-Salz der Stearinsäure. Die systematische Bezeichnung lautet Magnesiumdioctadecanoat:
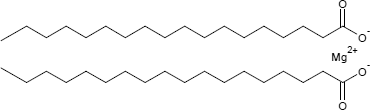
Das zweifach positiv geladene Mg2+-Ion bindet hierbei zwei Moleküle des einfach negativ geladenen Stearinsäure-Anions.
In reinem Substanz ist das Fettsäuresalz eine weiße, sich fettig anfühlende Substanz, die leicht nach Stearinsäure riecht, einen charakteristischen Geschmack aufweist, bei etwa 88 Grad Celsius schmilzt und in herkömmlichen Lösungsmitteln wie Wasser, Alkohol und Ether unlöslich ist. Lösen läßt sich das Salz in jeweils warmen Alkohol und Benzol.
Im Handel erhältliches Magnesiumstearat besteht meist aus Mischungen mit Magnesiumpalmitat und/oder geringen Beimengungen von Magnesiumsalzen anderer Fettsäuren. Als Verunreinigung ist darüber hinaus Magnesiumoxid zu finden. In kristalliner Form bildet es Mono-, Di- und Trihydrate.
Herstellung
Art und Umfang der im Magnesiumstearat anzutreffenden Verunreinigungen sind auf die industriellen Herstellungsprozesse zurückzuführen. Ausgangsmaterialien sind meist pflanzliche, aber auch tierische Fette, aus denen Stearin- und Palmitinsäure als Mischung gewonnen wird; diese wiederum werden mit Natronlauge (NaOH) zu den Natriumsalzen umgesetzt:
C17H35COOH + NaOH → C17H35COONa + H2O
.Die Synthese der Magnesiumstearats erfolgt schließlich durch Reaktion des Natriumstearats mit einem Magnesiumsalz wie zum Beispiel Magnesiumsulfat (Heptahydrat) oder Magnesiumchlorid:
2 C17H35COONa + MgSO4 x 7 H2O → Mg(C17H35COO)2 x n H2O ↓ + NaSO4 + 6 H2O.
Verwendung
Magnesiumstearat findet vielfach Anwendung als Verdünnungsmittel bzw. Füllmittel, Bindemittel und als Trägersubstanz bei der Herstellung von Tabletten, Kapseln und Pulvern etc. Die Substanz zeichnet sich durch ihre guten Schmier- und Antihafteigenschaften aus. Als Mischungsvermittler sorgt das Salz für das richtige Mischungsverhältnis in Arzneimitteln und Nahrungsergänzungsmitteln.
In kosmetischen Artikel erfüllt das gut an der Haut haftende Magnesiumstearat die Funktion einer Rieselhilfe bzw. eines Antibackmittels, eines Füllmittels, eines Feuchthaltemittels und/oder eines weißen Farbstoffs. Die Verwendung in Kosmetika ist unter Kennzeichnung des Produkts mit dem INCI-Namen Magnesium stearate zulässig.
Die in diesen Produkten verwendeten Mengen an Magnesiumstearat gelten gemeinhin als unschädlich für die Gesundheit.
Datenblatt: Magnesiumstearat
Quellen und weitere Informationen:
[1] - Magnesium Stearate.
CosIng, Europäische Stoffdatenbank für Inhaltsstoffe der Kosmetika.
[2] - K. D. Ertel, J. T. Carstensen:
Chemical, physical, and lubricant properties of magnesium stearate.
Journal of Pharmaceutical Sciences, (1988), DOI 10.1002/jps.2600770715.
[3] - Mehmet Gönen, Theresa O. Egbuchunam, Devrim Balköse, Fikret Inal, Semra Ülkü:
Preparation, Characterization and Applications of Magnesium Stearate, Cobalt Stearate and Copper Stearate.
Key Engineering Materials, (2014), DOI 10.1201/b16588-15.
Aktualisiert am 22.11.2018.
Permalink: https://www.internetchemie.info/chemie-lexikon/stoffe/m/magnesiumstearat.php
© 1996 - 2024 Internetchemie ChemLin