|
|
|
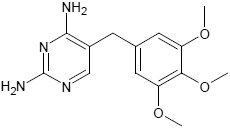
Das Antibiotikum Trimethoprim verbindet sich hoch spezifisch mit dem untersuchten Enzym; und über diese Behelfsbrücke lassen sich die Histone vom Typ 2B mit Farbstoffen markieren.
[Strukturformel: Trimethoprim; 2,4-Diamino-5-(3,4,5-trimethoxybenzyl)-pyrimidin]
[ InChI PZTPBGDSUXOBFF-UHFFFAOYAL ]
|
|
|
|
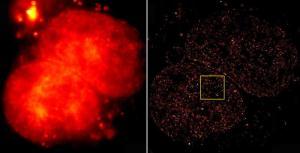
Gewaltiger Unterschied: Links eine herkömmliche Fluoreszenz-Aufnahme der 2B-Histone im Zellkern, rechts die superaufgelöste Variante, erstellt aus 10.000 Einzelaufnahmen mit der Methode dSTORM (direct stochastic optical reconstruction microscopy).
[Bilder: Arbeitsgruppe Markus Sauer, Biozentrum Uni Würzburg]
|
|
|
|
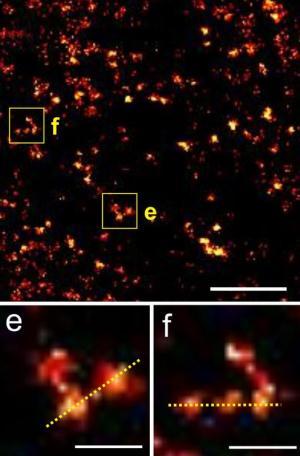
Mit Fluoreszenz-Farbstoffen markierte 2B-Histone im Kern einer lebenden Zelle: Oben ein Ausschnitt aus der vorherigen Abbildung, in der weiteren Vergrößerung (e, f) sind einzelne Histon-Moleküle erkennbar. Der weiße Messbalken entspricht 200 Nanometern.
[Abbildung: Arbeitsgruppe Markus Sauer, Biozentrum Uni Würzburg]
|
Optisch schaltbare Farbstoffe liefern schärfere Bilder Wer mit dem Fluoreszenz-Mikroskop zum Beispiel viele einzelne Proteine abbilden will, steht vor einer Herausforderung: Leuchten alle Proteine in der Zelle gleichzeitig auf, erscheint im Mikroskop nur ein verwaschener Lichtfleck. Grund: Die Proteine liegen zu nah beieinander, ihre Lichtsignale überlappen sich wie bei einem Kreuzfahrtschiff, auf dem in allen Kabinen das Licht an ist. Aus zu großer Entfernung sieht das Auge dann auch nur einen einzigen Lichtfleck. Würde man aber die Lichter an Bord einzeln und nur für kurze Zeit anschalten, ließe sich die Position jeder Kabine genau bestimmen. Falls sich das Schiff dabei bewegt, muss das natürlich schnell gehen, damit die Lichtsignale nicht verschmieren", sagt Markus Sauer. Genau diese Strategie wendet das Würzburger Team an - mit Fluoreszenz-Farbstoffen, die sich durch Lichtsignale an- und ausschalten lassen, die optisch schaltbar sind, wie die Forscher sagen. Damit ergeben sich deutlich schärfere Bilder von den Zuständen in der Zelle.
Lebende Zellen mit herkömmlichen Farbstoffen untersuchbar Optisch schaltbare Fluoreszenz-Farbstoffe versagen in lebenden Zellen, weil die Gegenwart von Sauerstoff stört das war die bislang vorherrschende Meinung in der Wissenschaft. Doch Sauers Team hat mit Kollegen in Bielefeld und New York nun erstmals gezeigt, dass das Gegenteil der Fall ist: Wir haben den Mechanismus durchschaut und wissen, dass es auch in lebenden Zellen geht. Wie dieser Mechanismus aussieht? Zellen enthalten Glutathion, das die meisten kommerziell verfügbaren optisch schaltbaren Farbstoffe nach der Laseranregung in einen stabilen, mehrere Sekunden dauernden Aus-Zustand versetzt. Zugleich läuft eine Reaktion mit Sauerstoff ab, welche die Farbstoffe wieder anschaltet, aber sehr ineffizient ist. Die Mehrzahl der Farbstoff-Moleküle ist darum ständig aus, und genau das ist die Voraussetzung, damit die superaufgelöste Bildgebung funktioniert, erklärt Professor Sauer.
Histone im Zellkern markiert Ihre Methodik exerzieren die Wissenschaftler in Nature Methods an den Histonen lebender menschlicher Zellen vor. Histone sind Proteine, mit deren Hilfe die DNA im Zellkern platzsparend verpackt wird. Fünf verschiedene Histone gibt es, mit der Variante 2B haben die Forscher gearbeitet. Zuerst koppelten sie die Histone vom Typ 2B an ein bakterielles Enzym (Dehydrofolatreduktase). Dann fügten sie den Fluoreszenz-Farbstoff dazu, den sie zuvor an das Antibiotikum Trimethoprim geknüpft hatten. Der Trick dabei: Das Antibiotikum verbindet sich hoch spezifisch mit dem Enzym; und über diese Behelfsbrücke lassen sich die Histone vom Typ 2B mit Farbstoffen markieren.
Nächster Schritt: Zellteilung beobachten Mit dieser Methode haben die Forscher eine bereits bekannte Tatsache bestätigt: Die mit Histonen verpackte DNA bewegt sich im Zellkern, und zwar abhängig von der Phase des Zellzyklus mit einer Geschwindigkeit von einigen Nanometern pro Sekunde. Sauer: Der nächste Schritt ist es jetzt, den Ablauf der Zellteilung in hoher Auflösung unter dem Mikroskop zu verfolgen.
|