Dichlordioxid - auch: Dichlorperoxid, Chlorperoxid, dimeres Chloroxid - ist eine anorganische Verbindung, der eine besondere Rolle bei der Zerstörung der atmosphärischen Ozonschicht zugeschrieben wird.
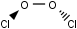
Dichlordioxid absorbiert ultraviolettes Licht mit einer maximalen Absorptionswellenlänge von 245 nm, in geringerem Maße aber auch längere Wellenlängen bis zu 350 nm; letzteres ist im Hinblick auf den atmosphärischen Abbau des Ozons in der Atmosphäre relevant, da Ozon bis zu 300 nm absorbiert.
Die Cl-O-Bindungslänge ist 170,4 Nanometer und die O-O-Bindung 1,426 nm lang. Der ClOO-Bindungswinkel beträgt 110,1°, der Diederwinkel zwischen den beiden Cl-O-O-Ebenen 81°.
Reaktionen
Das Chlormonoxid-Radikal, ClO, als Vorstufe des Dichlordioxids, bildet sich als Zwischenprodukt durch Photolyse oder Mikrowellenentladungen von Chlor-Sauerstoffgemischen (Ozon), durch Zerfall von Chlordioxid und Dichloroxid sowie durch andere Reaktionen. Die Dimerisierung zweier Chlormonoxid-Radikale führt zur Bildung des Dichlordioxids:
2 ClO →
Für die ozonschädigende Wirkung des Dichlordioxids in der Stratosphäre gilt folgender Reaktionsablauf [9]:
1. In einer Dreikörperreaktion wird aus Chlormonoxid und einem Katalysator M Dichlordioxid gebildet:
ClO + ClO + M → ClOOCl + M.
2. Die Einwirkung der ultravioletten Strahlung des Sonnenlichts bedingt die Photolyse des Dichloroxids zu ClOO-Radikalen und Chlor:
ClOOCl + hv → ClOO + Cl.
3. Das wenig stabile ClOO-Radikal wiederum zerfällt katalytisch hauptsächlich zu Sauerstoff und Chlor-Radikalen:
ClOO + M → Cl + O2 + M.
4. Die freiwerdenden Chlor-Radikale führen schließlich zum Ozonabbau; gleichzeitig werden Chlormonoxid-Radikale freigesetzt, die die Reaktion in Schritt 1 fortführen:
2[Cl + O3 → ClO + O2].
Datenblatt: Dichlordioxid
Quellen und weitere Informationen:
[1] - L. T. Molina, M. J. Molina:
Production of chlorine oxide (Cl2O2) from the self-reaction of the chlorine oxide (ClO) radical.
In: Journal of Physical Chemistry, (1987), DOI 10.1021/j100286a035.
[2] - R. A. Cox, G. D. Hayman:
The stability and photochemistry of dimers of the ClO radical and implications for Antarctic ozone depletion.
In: Nature, (1988), DOI 10.1038/332796a0.
[3] - James B. Burkholder et al.:
Ultraviolet absorption cross sections of chlorine oxide (Cl2O2) between 210 and 410 nm.
In: Journal of Physical Chemistry, (1990), DOI 10.1021/j100365a033.
[4] - W. B. DeMore, E. Tschuikow-Roux:
Ultraviolet spectrum and chemical reactivity of the chlorine monoxide dimer.
In: Journal of Physical Chemistry, (1990), DOI 10.1021/j100378a046.
[5] - K. J. Huder, W. B. DeMore:
Absorption cross sections of the ClO dimer.
In: Journal of Physical Chemistry, (1995), DOI 10.1021/j100012a007.
[6] - Teresa A. Moore, Mitchio Okumura:
UV Photolysis of ClOOCl.
In: Journal of Physical Chemistry A, (1999), DOI 10.1021/jp984410.
[7] - William J. Bloss et al.:
Kinetics of the ClO Self-Reaction and 210 nm Absorption Cross Section of the ClO Dimer.
In: Journal of Physical Chemistry A, (2001), DOI 10.1021/jp012429y.
[8] - J. R. McKeachie et al.:
Observation of a Heterogeneous Source of OClO from the Reaction of ClO Radicals on Ice.
In: Journal of Physical Chemistry B, (2004), DOI 10.1021/jp049314p.
[9] - Francis D. Pope et al.:
Ultraviolet Absorption Spectrum of Chlorine Peroxide, ClOOCl.
In: Journal of Physical Chemistry A, (2007), DOI 10.1021/jp067660w.
[10] - Marc von Hobe et al.:
The UV/Vis absorption spectrum of matrix-isolated dichlorine peroxide, ClOOCl.
In: Phys. Chem. Chem. Phys., (2009), DOI 10.1039/b814373k.
[11] - Dimitrios K. Papanastasiou et al.:
UV Absorption Spectrum of the ClO Dimer (Cl2O2) between 200 and 420 nm.
In: Journal of Physical Chemistry A, (2009), DOI 10.1021/jp9065345.
[12] - David M. Wilmouth et al.:
Chlorine-Catalyzed Ozone Destruction: Cl Atom Production from ClOOCl Photolysis.
In: Journal of Physical Chemistry A, (2009), DOI 10.1021/jp9053204.
[13] - Bing Jin et al.:
Photodissociation Cross Section of ClOOCl at 330 nm.
In: Journal of Physical Chemistry A, (2010), DOI 10.1021/jp909374k.
[14] - G. Wetzel et al.:
First remote sensing measurements of ClOOCl along with ClO and ClONO2 in activated and deactivated Arctic vortex conditions using new ClOOCl IR absorption cross sections.
In: Atmospheric Chemistry and Physics, (2010), DOI 10.5194/acp-10-931-2010.
[15] - NN:
Dichlordioxid als Schlüsselverbindung des Ozonabbaus identifiziert.
In: Internetchemie News, (2010).
Aktualisiert am 21.11.2018.
Permalink: https://www.internetchemie.info/chemie-lexikon/stoffe/d/dichlordioxid.php
© 1996 - 2026 Internetchemie ChemLin