Stickstoff zählt zu den Grundbausteinen des Lebens. Von der begrenzten Verfügbarkeit des molekularen Stickstoffs N2 ist auch das Pflanzenwachstum abhängig.
Für die Landwirtschaft ist das ein Problem. Aus diesem Grund wird mit dem Haber-Bosch-Verfahren der Ammoniaksynthese künstlicher Stickstoffdünger hergestellt.
Dieses Verfahren benötigt bei der derzeitigen Produktionsmenge etwa ein Prozent der gesamten globalen Energieproduktion.
In der Natur findet sich dafür eine biologische Lösung: Einem Forscherteam um Prof. Dr. Oliver Einsle, Institut für Organische Chemie und Biochemie der Universität Freiburg und Mitglied des Exzellenzcluster BIOSS, ist es gelungen, einen wichtigen Teil dieser Lösung aufzudecken.
Ihre Erkenntnisse wurden im Fachmagazin Science veröffentlicht [siehe unten].
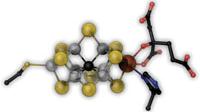
Das bakterielle Enzym Nitrogenase kann die chemische Reaktion von N2 zu Ammonium katalysieren - es ist die natürliche Version des Haber-Bosch-Verfahrens. Im Zentrum der Nitrogenase findet sich ein Metallcluster, der Eisen-Molybdän-Cofaktor (FeMoco), an dem die chemische Aktivierung des Substrats N2 stattfindet. Bisher war nicht nachvollziehbar, wie diese Aktivierung im Detail abläuft und welches chemische Element dem Atom im Metallcluster zuzuordnen ist. Deswegen konnte auf Basis des FeMoco noch kein effizienterer Katalysator für die industrielle Stickstoffherstellung entwickelt werden.
Die Freiburger Wissenschaftlerinnen und Wissenschaftler haben zusammen mit Arbeitsgruppen vom Freiburger Institut für Physikalische Chemie, dem California Institute of Technology in Pasadena/USA, dem Max-Planck-Institut für Bioanorganische Chemie in Mühlheim an der Ruhr und der University of California in Irvine/USA gezeigt, dass es sich bei dem zentralen Atom des Metallclusters um Kohlenstoff handelt. Diese Erkenntnis wird von großer Bedeutung für das Verständnis der Biogenese und der Funktionalität des Metallclusters sein:
Da die Wissenschaftler nachgewiesen haben, dass der FeMoco einen Kern aus Kohlenstoff hat, rückt die Möglichkeit eines Nachbaus des Enzyms zur energiesparenden Herstellung von Stickstoffdünger näher.
Zusatzinformationen:
Thomas Spatzal, Müge Aksoyoglu, Limei Zhang, Susana L. A. Andrade, Erik Schleicher, Stefan Weber, Douglas C. Rees, Oliver Einsle:
Evidence for Interstitial Carbon in Nitrogenase FeMo Cofactor.
In: Science; Vol. 334, Nr. 6058, Seite 940, online veröffentlicht am 18. November 2011, DOI 10.1126/science.1214025
Quelle: Albert-Ludwigs-Universität, Freiburg im Breisgau
Aktualisiert am 22.11.2011.
Permalink: https://www.internetchemie.info/news/2011/nov11/eisen-molybdaen-cofaktor.php
© 1996 - 2026 Internetchemie ChemLin