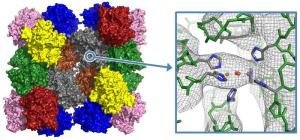
Der Kaiserskorpion (Pandinus imperator) gehört nicht nur zu den größten Skorpionen überhaupt, sondern fällt auch durch die ungewöhnliche Größe eines Proteins aus dem Rahmen. Sein Blutfarbstoff Hämocyanin ist ein Proteinkomplex aus 24 Untereinheiten und gehört zu den größten Proteinen - vergleichbar mit dem Ribosom oder sogar kleinen Viren.
Wissenschaftlern der Johannes Gutenberg-Universität Mainz (JGU) ist es nun erstmals gelungen, Kristalle des Kaiserskorpion-Hämocyanins zu züchten. Damit kann eine genaue Strukturanalyse mithilfe von Röntgenstrahlen durchgeführt werden. Bisher werden sehr große Proteinstrukturen wie die des Hämocyanins meist durch Elektronenmikroskopie untersucht, die allerdings aus methodischen Gründen keine Auflösung erreichen, um einzelne Atome zu unterschieden.
Mit der Röntgenkristallographie kann die Struktur von Proteinen jedoch noch genauer erforscht und im günstigsten Fall die räumliche Anordnung einzelner Atome ermittelt werden. Das ist die Voraussetzung, um zu verstehen, wie diese riesigen Proteinkomplexe funktionieren.
Hämocyanine sind außerordentlich große Atmungsproteine, die bei Weichtieren und Gliederfüßern den Sauerstoff im Blut transportieren. Der Sauerstoff bindet bei diesen blauen Blutproteinen zwischen 2 Kupferatomen, während er bei Menschen in den roten Blutkörperchen an Eisen andockt. Das Faszinierende an Hämocyanin ist für die Biologen, dass zur Aufnahme von Sauerstoff, für seinen Transport und die Abgabe je nach Tierart bis zu 160 Sauerstoffbindungszentren in einem Proteinkomplex miteinander kommunizieren. Diese als Kooperativität bezeichnete Eigenschaft, die bspw. in der Nanotechnologie angewendet werden könnte, um molekulare Schalter zu bauen, ist in der Natur einmalig - und kann im Detail nur durch Strukturaufklärung mit atomarer Auflösung verstanden werden.
Am Institut für Biophysik der JGU ist es nun Prof. Dr. Elmar Jaenicke erstmals gelungen, den blauen Hämocyanin-Proteinkomplex des Kaiserskorpions zu kristallisieren. Dies ist der entscheidende 1.Schritt zur Röntgenstrukturaufklärung, denn Kristalle sind die Voraussetzung dafür, dass die Röntgenstrahlung richtig gebeugt wird und die Struktur entschlüsselt werden kann. Die Kristallisation ist bei sehr großen Proteinkomplexen besonders schwierig. "Es ist ein bisschen ein Glücksspiel", sagt Jaenicke über das Kristallisationsverfahren, das von vielen Faktoren, wie z.B. dem ph-Wert, dem Salzgehalt der Lösung und der Temperatur, abhängig ist. "Der entscheidende Schritt ist immer die Bildung eines Kristallisationskeims." Jaenicke zufolge kann das allerdings Monate dauern und erfordert viel Geduld. Manchmal zieht sich die Optimierung der Kristallisationsbedingungen über mehrere Jahre hin. Dies ist auch der Grund, warum bisher weltweit nur eine Handvoll Strukturen von sehr großen Proteinkomplexen mit Röntgenstrukturaufklärung gelöst wurde. Eine davon, die des Ribosoms, wurde 2009 mit dem Nobelpreis ausgezeichnet.
Die Kristalle werden im Röntgenstrahl vermessen und die Struktur in einem aufwendigen Verfahren aus der gestreuten Röntgenstrahlung berechnet. Im Fall des Kaiserskorpion-Proteins gelang es den Wissenschaftlern um Jaenicke vorerst, eine Struktur mittlerer Auflösung (6,5 Ångström) zu erhalten, bei der man Sekundärstrukturelemente wie a-Helices sehen kann, aber bspw. noch keine einzelnen Aminosäuren. Zum Vergleich: Wäre das Protein ein Backsteinhaus und man würde seine Struktur aus großer Entfernung mit dem Fernrohr ermitteln wollen, dann wären bei der jetzigen Auflösung Fenster, Türen und auch der Briefkasten sichtbar, aber noch nicht die Lage von einzelnen Backsteinen. "Wir haben einen Anfangspunkt gesetzt und können jetzt schon Teile des aktiven Zentrums des Moleküls sehen. Nun sind wir auf dem Weg, mit einer weiteren Verbesserung unserer Kristalle auch eine atomare Auflösung zu erzielen, was mit keiner anderen Methode möglich ist." Laut Jaenicke würde das Sauerstoffbindungsprotein des Kaiserskorpions dann zu den 5 größten Strukturen gehören, die bis heute mit Röntgenstrukturanalyse aufgeklärt worden sind.
An der Johannes Gutenberg-Universität Mainz besteht eine ideale Infrastruktur zur Strukturforschung an sehr großen Proteinkomplexen, die in dieser Form nur an wenigen Forschungseinrichtungen weltweit betrieben werden kann. Dabei wird mit der Röntgenstrukturaufklärung am Institut für Molekulare Biophysik (AG Decker, AG Jaenicke) der atomare Auflösungsbereich und mit der Cryo-Elektronenmikroskopie am Institut für Zoologie (AG Markl) der mittlere Auflösungsbereich abgedeckt. Die am Institut für Molekulare Biophysik verwendete neue Röntgen-Drehanode produziert fokussierte Röntgenstrahlung, die von der Intensität mit einer Synchrotron-Beamline der 2. Generation vergleichbar und somit ideal geeignet ist, um in die Struktur von Riesenmolekülen vorzudringen.
Zusatzinformationen:
Elmar Jaenicke, Bruno Pairet, Hermann Hartmann, Heinz Decker:
Crystallization and Preliminary Analysis of Crystals of the 24-Meric Hemocyanin of the Emperor Scorpion (Pandinus imperator).
In: PLoS One; online veröffentlicht am 05. März 2012, DOI 10.1371/journal.pone.0032548
Quelle: Johannes Gutenberg-Universität, Mainz
Aktualisiert am 24.06.2012.
Permalink: https://www.internetchemie.info/news/2012/jun12/haemocyanin-kristallisation.php
© 1996 - 2026 Internetchemie ChemLin