Benzaldehyd ist eine organisch-chemische Verbindung aus der Gruppe der aromatischen Aldehyde (Arencarbaldehyde), d. h., dass Molekül besteht aus einer Benzol-Ringstruktur, die die aromatischen Eigenschaften trägt, und einer Aldehyd-Gruppe (Formyl-Gruppe), die an den Ring substituiert ist.
Bezeichnungen und Identifikatoren
Benzaldehyd
C7H6O
106,124 (g/mol)
100-52-7
202-860-4
HUMNYLRZRPPJDN-UHFFFAOYSA-N
Weitere Bezeichnungen, Synonyme
Benzenaldehyd; Benzencarbaldehyd; Benzolcarbaldehyd; Phenylmethanal
INCI-Bezeichnung
Benzaldehyde
Englische Bezeichnung
Benzaldehyde
Benzenecarbaldehyde; Benzenecarboxaldehyde; Phenylmethanal; Benzoic aldehyde
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Benzaldehyd:
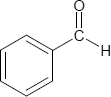
C7H6O
Mr = 106,124 g/mol
SMILES: c1ccc(cc1)C=O
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Benzaldehyd. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
In reinem Zustand ist Benzaldehyd eine farblose, stark lichtbrechende Flüssigkeit, die einen an Bittermandeln erinnernden Geruch aufweist, wenig in Wasser löslich ist und sich bei der Lagerung mit der Zeit gelblich, später braun verfärbt und an der Luft langsam zu Benzoesäure oxidiert.
+ Löslich in Alkohol, Ether, Ölen.
- In Wasser schwer löslich (6,95 g/L bei 25 °C).
- Verteilungskoeffizient logPOW = 1,4 bei 25 °C.
-26 °C
179 °C
62 °C
192 °C
1,05 g cm-3 bei 20 °C
pK1s = 14,90 bei 20 °C
1,26 hPa bei 20 °C
1,321 mPa s bei 20 °C
70,5 mN/m bei 20 °C
nD = 1,5446 bei 20 °C
-36,8 kJ/mol bei 25 °C
-3525,0 kJ/mol bei °C
-60,78 × 10-6 cm3 mol-1
Spektroskopische Daten:
splash10-0a6r-9600000000-731755b6449c9d44f340
splash10-004i-9100000000-ce8274b57c274e79f894
splash10-056r-9400000000-d5e049f5a5c77b8864cb
splash10-0a4i-0900000000-ae1e0ddb2c355ea94682
Berechnetes NMR-Spektrum (Predict Spectra via NMRDB)
1H NMR Spektrum, 13C NMR Spektrum.
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Benzaldehyd - C7H6O - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Kohlenstoff
ΣAr = 84,077 u
12C: 12 u [98,94 %]
13C: 13,00335 u [1,06 %]
14C: 14,00324 u [<< 1 %]
12C: 78,38546 %
13C: 0,83979 %
14C: Spuren
Wasserstoff
ΣAr = 6,048 u
1H: 1,00783 u [99,99 %]
2H: 2,0141 u [0,01 %]
3H: 3,01605 u [<< 1 %]
1H: 5,69842 %
2H: 0,00057 %
3H: Spuren
Sauerstoff
16O: 15,99491 u [99,757 %]
17O: 16,99913 u [0,03835 %]
18O: 17,99916 u [0,205 %]
16O: 15,03913 %
17O: 0,00578 %
18O: 0,03091 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 106,124 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 9,423 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,009 mol.
Monoisotopische Masse: 106,0418648122 Da - bezogen auf 12C71H616O.
Vorkommen
Benzaldehyd ist der Hauptbestandteil (etwa 95 % ) von Bittermandelöl - ein etherisches Öl aus den Steinkernen bzw. Samen verschiedener Prunus-Arten - und kann daraus und aus einer Reihe anderer natürlicher Quellen gewonnen werden.
Die Kerne von Mandeln, Aprikosen, Äpfeln, Kirschen u. a. enthalten erhebliche Mengen des Glykosids Amygdalin, das unter Enzymkatalyse in Benzaldehyd, Cyanwasserstoff (Blausäure) und zwei Äquivalente D-Glucose zerfällt, wobei diese Substanzen freigesetzt werden.
Benzaldehyd trägt auch als Komponente zum Duft von Austernpilzen (Pleurotus ostreatus) bei.
Synthese, Gewinnung
Die Dampfphasenoxidation von Toluol war der dominierendeToluol-Oxidationsprozess in den 1950er und frühen 1960er Jahren, ist heute aber nicht mehr von industrieller Bedeutung.
Heuzutage ist die Luftoxidation von Toluol die Quelle des größten Teils des weltweit synthetisch hergestellten Benzaldehyds. Es werden sowohl Dampf- als auch Flüssigphasen-Luftoxidationsverfahren verwendet. Bei dem Dampfphasenverfahren wird ein Gemisch aus Luft und Toluoldampf über einen Katalysator geleitet, der aus den Oxiden von Uran, Molybdän oder anderen Metallen besteht. Hohe Temperaturen und kurze Kontaktzeiten sind erforderlich, um die Ausbeuten zu maximieren. Dem Katalysatorgemisch können kleine Mengen Kupfer(II)-oxid zugesetzt werden, um die Bildung von Maleinsäureanhydrid als Nebenprodukt zu verringern.
Im Flüssigphasenverfahren werden sowohl Benzaldehyd als auch Benzoesäure gewonnen.
Benzaldehyd ist in zwei Qualitäten im Handel erhältlich. Reiner Benzaldehyd, der für die meisten Anwendungen geeignet ist, macht mehr als 95% der verkauften Menge aus. Doppeldestillierter - und damit reinerer - Benzaldehyd wird hauptsächlich in der Pharma-, Parfüm- und Aromaindustrie verwendet.
Verwendung in Lebensmitteln
Benzaldehyd wird in den USA allgemein als sicherer Lebensmittelzusatzstoff (GRAS) angesehen und ist in der Europäischen Union als Aromastoff anerkannt. Die Substanz wird üblicherweise verwendet, um Lebensmitteln und duftenden Produkten Mandelgeschmack bzw. ein Marzipan-Aroma zu verleihen.
Verwendung in Kosmetika
INCI-Bezeichnung: Benzaldehyde
Benzaldehyd ist in kosmetischen Produkten und Parfüms als denaturiernder, geruchsmaskierender, aromatischer und duftender Inhaltsstoff zugelassen. Gewöhnlich enhalten die wenigen Benzaldehyd-haltigen Produkten weniger als 0,5 % der Substanz.
Quelle: CosIng (Cosmetic Ingredient Database der EU) Nummer: 74599.
Duftstoff, Aromastoff
Künstliches Bittermandelöl, an Marzipan erinnerndes Aroma.
Benzaldehyd ist als Aromastoff und/oder Duftstoff in den einschlägigen Listen aufgeführt (siehe folgende Identifikatoren).
EU-Vorschriften: Siehe Datenbank für Lebensmittelaromen Ref.-Nr. 3742 (EU Food Flavourings Database)
05.013
22
2127
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)

Signalwort: Achtung
Gefahrenhinweise (H-Sätze):
- H302
Gesundheitsschädlich bei Verschlucken.
LD50 (Ratte, oral): 1300 mg/kg. LD50 (Maus, oral): 28 mg/kg.
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.002.601 sowie Informationen zu REACh unter ECHA Chem 100.002.601.
Zur Toxikologie und zum Arbeitsschutz beim Umgang mit Benzaldehyd sowie Maßnahmen im Gefahrenfall siehe: Gefahrstoffinformationssystem GESTIS, ZVG-Nr. 013380.
Hinweis: Die Kennzeichnungspflicht gemäß CLP-Verordnung gilt unter anderem nicht für bestimmte Stoffe und Gemische für Endverbraucherinnen und Endverbraucher, die in Form von Fertigerzeugnissen vorliegen, wie zum Beispiel Arzneimittel, Tierarzneimittel, Kosmetika, bestimmte Medizinprodukte und medizinische Geräte, Lebensmittel oder Futtermittel sowie bestimmte Lebensmittelzusatzstoffe oder Aromastoffe. Hier sind gegebenenfalls gesonderte rechtliche Vorschriften einzuhalten.
Externe Informationsquellen
Hersteller und Bezugsquellen
Benzaldehyd als kommerzielles Produkt von international tätigen Lieferanten und Suche nach Analoga siehe unter: ZINC000000895145.
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Benzaldehyd als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[0] - Fach- und Forschungsartikel in wissenschaftlichen Zeitschriften via PubMed: Benzaldehyde.
[1] - NN:
Final Report on the Safety Assessment of Benzaldehyde.
In: International Journal of Toxicology, (2006), DOI 10.1080/10915810600716612.
Letzte Änderung am 07.07.2024.
Permalink: https://www.internetchemie.info/substanz/Benzaldehyd.php
© 1996 - 2026 Internetchemie ChemLin